9023 溶解度测量指导原则
溶解是两种或两种以上物质混合形成均匀相的过程,通常是指溶质与溶剂混合形成溶液的过程。溶解度是药物的一种物理性质,指溶质均匀地溶解在溶剂中的程度,也反映溶剂溶解溶质的能力。溶解度可以用不同的浓度单位表示,如摩尔浓度、摩尔分数、摩尔比、质量/体积、质量/质量等。溶解度有以下三种表示方法。
平衡溶解度:也称为热力学溶解度,是指在热力学平衡状态下,存在未溶解固体时,溶质在溶剂中达到的极限浓度。在一定时间范围内,浓度数值不再发生显著变化,表明体系已达到平衡状态。
表观溶解度:是在溶剂体系未达到平衡状态或无法验证平衡时,根据经验确定的溶解度。在瞬时过饱和或由于时间不足以达到平衡而导致溶解不完全的情况下,表观溶解度可能高于或低于平衡溶解度。
特性溶解度:也称为固有溶解度,即不带电荷分子的溶解度,是指药物在溶剂中不发生解离或缔合,也不与溶剂中的其他物质发生相互作用时,所形成的饱和溶液的浓度。特性溶解度通常在不带电荷分子为主的pH值范围内测量。对于某些化合物,特性溶解度无法直接测量,需要通过将溶解度数据作为pH值的函数进行拟合,或者利用相溶原理图来确定。
溶解度可以通过绝对值和相对值两种方式来描述。在凡例中描述的是近似溶解度,这是一种以绝对值表示的方法,根据溶解程度的不同划分为不同级别,包括极易溶解、易溶、溶解、略溶、微溶、极微溶解、几乎不溶或不溶。生物药剂学分类系统(BCS)则采用相对溶解度的概念,将药物分为高溶解性和低溶解性,这对于药物的剂型选择和制剂开发具有重要意义。
准确测量药物的溶解度对于理解药物制剂的质量控制和药物递送至关重要。药物的溶解度受到多种因素的影响,包括药物的理化性质(如表面积、颗粒大小、晶体形态)、溶解介质的性质(如pH值、极性、表面张力、添加的表面活性剂、潜溶剂、盐),以及溶解度测量参数设置(如温度、时间、搅拌方法)。此外,表观溶解度可能包括不带电荷部分的特性溶解度、电离化合物的溶解度,以及增溶剂和不同晶型或盐型的作用下的溶解度。在溶解度测量过程中,控制这些实验因素是获得准确且可靠的溶解度数值的关键。
一、水中的溶解度估算方法
水中的溶解度是指溶质在以水为主要溶解介质中的溶解度,它可能受到潜溶剂、表面活性剂、络合剂、pH值或其他共溶质的增溶作用的影响,因此水中的溶解度在很大程度上受溶解介质组成的影响。
一般溶解度方程可用于估算化合物在水中的特性溶解度,计算公式如下:
lgS0=0.5-0.01(MP-25)-lgKOW
式中 S0为特性溶解度(即非离子化分子的溶解度);
MP为结晶固体的熔点(单位:℃);
KOW为正辛醇-水分配系数,水温为25℃。
上述方程表明,具有较高熔点和亲油性的化合物在水中的溶解度往往较低。正辛醇-水分配系数的对数反映了由于混合焓导致的理想溶液与水溶液之间的差异。如果化合物的pKa值已知,一般溶解度方程还可以与亨德森-哈塞尔巴尔赫方程结合使用,以预测离子化合物的溶解度(见“二、1 pH值的影响”)。
使用一般溶解度方程时需要测定化合物的熔点和分配系数,对于离子化合物还需测定pKa值。目前,有几种计算机软件能够基于化合物的结构估算分配系数和pKa值,但这些软件通常不适用于预测熔点。开发用于预测水中的溶解度计算方法通常依赖于分子训练集,以寻找与那些从结构上更容易预测的性质之间的相关性,例如分子量、溶剂可及表面积、可旋转键的数量等。尽管这些计算方法可以成功应用于与训练集相似的分子,在预筛选合成候选物方面有一定帮助,但它们的准确性有限,不能完全替代实验测定的溶解度。
二、影响溶解度和溶解度测量的因素
1 pH值的影响
带电物质比中性物质对水有更高的亲和力,因此可电离酸或碱的溶解度具有pH值依赖性。可电离酸或碱的总溶解度是其特性溶解度与在该pH值下存在的电离溶质的量之和。亨德森-哈塞尔巴尔赫方程将溶液的pH值与可电离酸或碱的pKa值联系起来,并描述了溶解度随pH值变化的关系。
对于弱酸,其总溶解度可按下式计算:
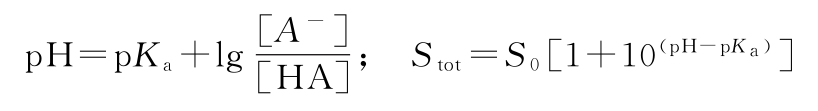
式中 pKa为-lgKa;
Ka为酸解离常数;
[A-]为酸的共轭碱的摩尔浓度;
[HA]为未解离弱酸的摩尔浓度;
Stot为弱酸的总溶解度;
S0为不带电部分的特性溶解度。
对于弱碱,其总溶解度可按下式计算:
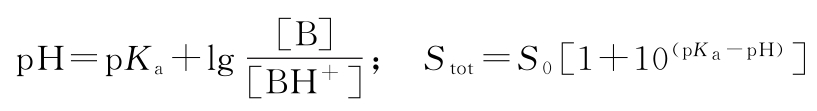
式中 pKa为-lgKa;
Ka为碱解离常数;
[B]为碱的共轭酸的摩尔浓度;
[BH+]为解离碱的摩尔浓度;
Stot为弱碱的总溶解度;
S0为不带电部分的特性溶解度。
亨德森-哈塞尔巴尔赫方程有助于解释在第一个pKa值时溶解度的增加,但它不适用于模拟含有多个pKa值的pH值范围内多元酸的行为。由于可电离分子在可电离基团的数量和类型上可能存在差异,因此研究在特定pH值范围内的溶解度变化是十分重要的。图1展示了一个具有两个pKa值(5.6和11.7)的分子的溶解度如何随pH值的变化而变化。该分子在pH值低于5.6或高于11.7时带电,在这两个pH值之间则表现为中性。当分子处于中性状态时,其溶解度等于其特性溶解度。对于可电离分子,溶解度会随着pH值的变化而呈对数增长。盐的形成可能在低pH值或高pH值范围抑制溶解并降低溶解度(图1)。如果用来调节pH值的酸为形成的盐提供了反离子,那么随着反离子浓度的增加,同离子效应可能会进一步降低溶解度(图1中pH<2的情况)。如果盐在较高的pH值下溶解,溶液可能最初会过饱和,但由于任何固体形态在该pH值下的溶解度都更低,最终会形成沉淀。
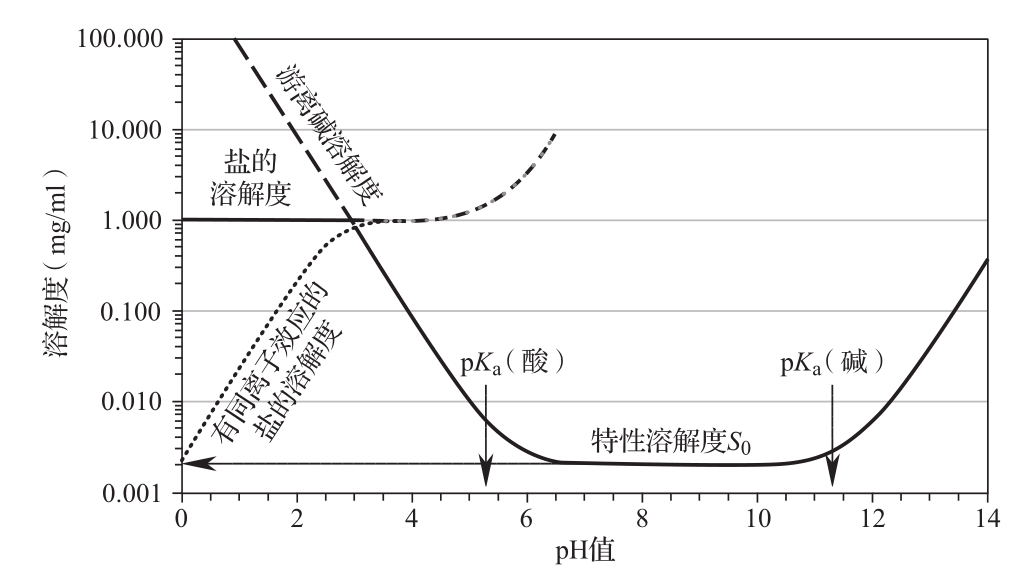
图1 pH值对可电离化合物溶解度的影响
2 盐和反离子的影响
可电离化合物可以与带相反电荷的反离子形成盐。在含有带电反离子的溶液中,溶度积(Ksp)描述了这种平衡反应,公式如下:
盐的溶解:AnBm(s)→nA+(aq)+mB-(aq)
溶度积:Ksp=[A+]n[B-]m
盐在溶液中的最大溶解度如图1所示。由于盐的形成,带电分子的实际溶解度趋于稳定(本例中pH值低于药物的pKa值),这与亨德森-哈塞尔巴尔赫方程预测的溶解度随pH值变化而持续增加的情况不同。Ksp是一个常数,因此如果用来调节pH值的酸增加了带相反电荷的反离子的浓度,那么可电离部分的溶解度可能会进一步下降。随着反离子浓度的增加,带电分子的溶解度降低,这种现象被称为同离子效应。例如,在使用盐酸降低pH值时,由于氯离子浓度的增加,氯盐的溶解度会降低(比如pH<2时)。虽然图1没有明确指出,但盐也可能限制碱性一侧的溶解度(例如酸的钠盐),当用于调节pH值的化合物具有同离子(例如氢氧化钠)时,同离子效应也可能影响高pH值下的溶解度。
3 潜溶剂的影响
为了提高难溶性药物的溶解度,常使用两种或多种混合溶剂。在特定的混合比例下,药物的溶解度可能达到极大值,这种现象称为潜溶,这样的溶剂被称为潜溶剂。可与水混溶的潜溶剂有乙醇、丙二醇、聚乙二醇等。根据对数线性模型,溶质的溶解度对数通常可以在两种可混溶的潜溶剂之间进行线性插值(图2)。当这个溶解度图转换至线性标尺时,明显地显示出,即使在潜溶剂混合物中只含有低浓度的不良溶剂(通常是水),也能显著降低溶质的溶解度。因此,由于溶解度的显著变化,稀释含有潜溶剂的溶液时溶质特别容易析出。
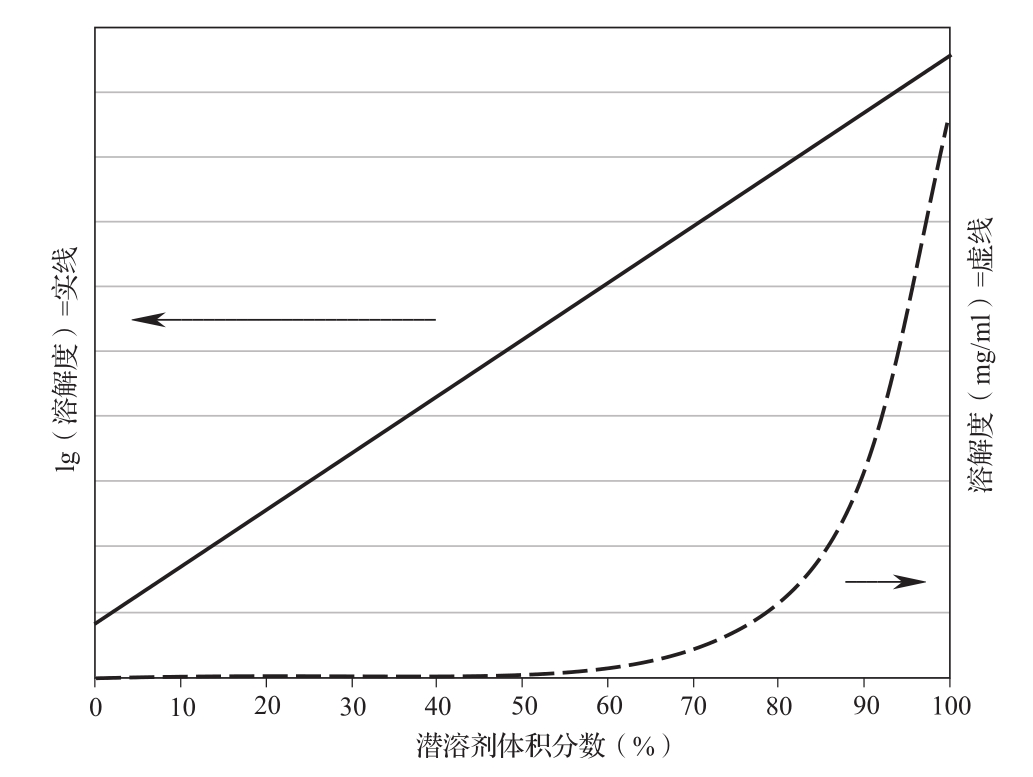
图2 对数线性模型示意图
注:如图2所示,这个简单的模型假设当潜溶剂的比例达到100%时,溶解度达到最大值,但并非所有潜溶剂体系都遵循这一假设。
4 表面活性剂的影响
表面活性剂是一种两亲性物质,具有极性和非极性基团。当置于水中时,表面活性剂倾向于驻留在空气-水界面,将极性基团朝向水,非极性基团朝向空气(即极性较小的区域)。当空气-水界面的表面活性剂吸附达到饱和后,额外的表面活性剂分子会聚集形成球形胶束,这些胶束内部是非极性疏水空间,由亲油基团排列而成;外部是亲水基团形成的极性区。胶束形成时的浓度称为临界胶束浓度(CMC),在CMC以上,溶液中的胶束数量随着表面活性剂浓度的增加而线性增加。如果药物分子能够进入胶束,其溶解度将随着胶束数量的增加而线性增加(图3)。表面活性剂的CMC受温度、离子强度和pH值等因素的影响。例如,在25℃纯水中,十二烷基硫酸钠的CMC约为6mmol/L,而聚山梨酯80的CMC约为0.012mmol/L。表面活性剂对药物分子的增溶作用可以通过两个参数来评估:摩尔增溶能力和胶束-水分配系数。胶束-水分配系数是在特定表面活性剂浓度下,胶束中药物浓度与水中药物浓度的比值。
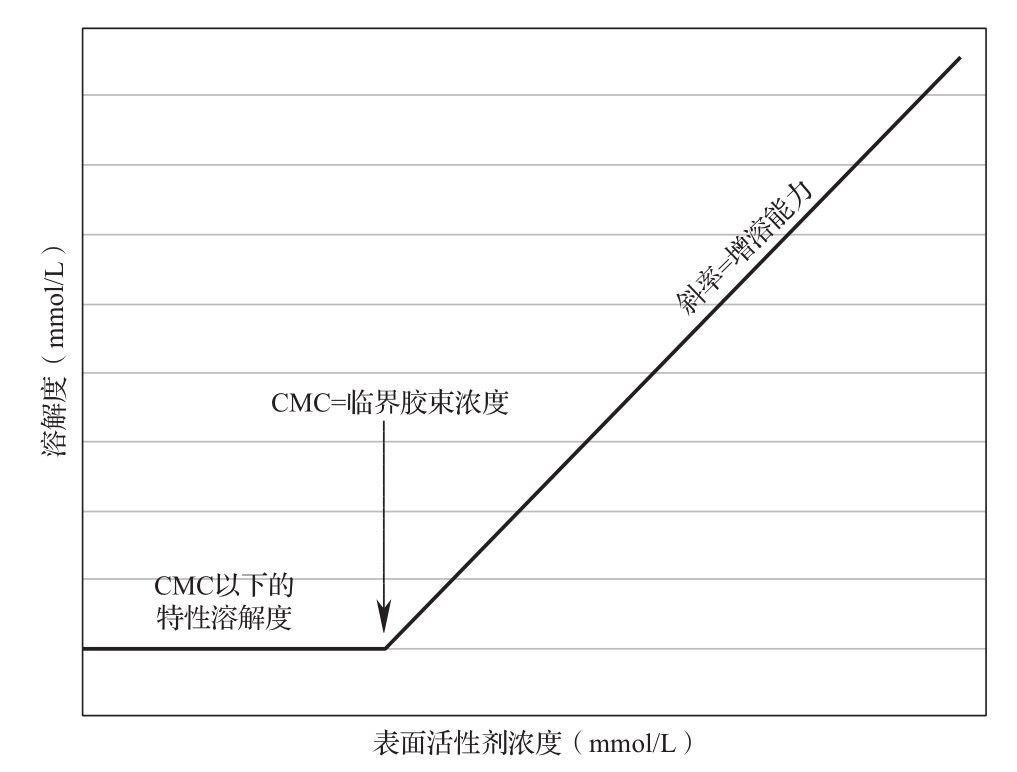
图3 通过表面活性剂增加溶解度的示意图
如图3所示,表面活性剂通过形成胶束实现增溶作用。在CMC以下,加入的表面活性剂以单体形式溶解在溶剂中,此时药物的溶解度没有增加。然而一旦超过CMC,药物的溶解度会随着表面活性剂浓度的增加而线性增长。这种线性增长的斜率反映了胶束的增溶能力。在表面活性剂存在的情况下,药物的溶解度是水相中直接溶解的药物量与胶束中溶解的药物量之和。由于胶束的体积比溶质大,它们在溶液中的扩散速度比溶质慢。存在胶束时的药物递送不仅依赖于溶液中游离药物的吸收,还包括胶束介导的递送过程。因此,表面活性剂的增溶作用可能不会使药物递送效率与水溶性的提高呈正比例增强。
5 络合剂的影响
络合剂能与难溶物质形成分子间络合物,提高难溶性药物在水中的溶解度。在络合剂的作用下,非极性分子与络合剂的非极性基团被隔离出水相,从而改善了非极性分子的水溶性,使水溶液能够容纳更多的非极性分子。溶解度会随络合剂浓度的增加而增加,这与表面活性剂的增溶作用类似,但络合作用不要求特定的最小浓度。具有高稳定常数的络合物可以与溶质紧密结合,增强水溶液的稳定性。环糊精是一种常用的络合剂,通过与原料药形成络合物提高其溶解度。
6 表面积的影响(溶解速度)
固体药物的溶解速度主要由扩散过程控制,这可以用Noyes-Whitney方程来描述,公式如下:
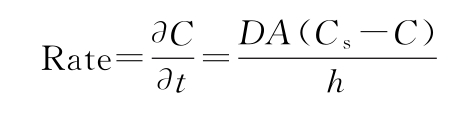
式中 C为在时间t时,溶质在溶剂中的浓度;
D为溶质的扩散系数;
A为溶质颗粒的表面积;
Cs为溶质的饱和溶解度;
h为扩散层的厚度。
在未搅拌的溶液中,h可能较大,此时药物的溶解速度主要受到D的影响。搅拌可以显著减小h的值,从而加快溶解速度。扩散层厚度越大,溶解速度越慢;搅拌速度快时,扩散层变薄,溶解速度加快。对于在充分混合的溶液中的小颗粒,h与颗粒半径的平方根成正比,这意味着颗粒越小,其表面积越大,溶解速度越快。为了尽快达到平衡溶解度,应尽可能增加溶质颗粒的表面积(即减小颗粒大小),并通过加强搅拌减小扩散层的厚度。虽然药物的溶解速度不会影响平衡溶解度,但会影响达到平衡所需的时间。
7 表面能的影响
颗粒的表面能可能影响溶解度。根据开尔文方程,表面能对体系的总吉布斯自由能有影响,使得小颗粒比大颗粒具有更高的溶解度。这种尺寸对溶解度的影响通常在颗粒直径小于1μm时才显著。开尔文方程的公式如下:
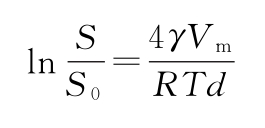
式中 S为表观溶解度;
S0为无限大颗粒的溶解度;
γ为溶质的表面能;
Vm为溶质的摩尔体积;
R为气体常数;
T为温度;
d为颗粒的直径。
小颗粒和大颗粒之间的溶解度差异会导致分散悬浮液中发生奥斯瓦尔德熟化现象。在这个过程中,小颗粒溶解,形成相对于大颗粒的溶解度而言的过饱和溶液,这促使大颗粒表面的再结晶。大颗粒尺寸增大,小颗粒溶解,最终导致悬浮液中的平均颗粒尺寸增加。
三、溶解度测量方法
1 平衡溶解度测定方法——摇瓶法
摇瓶法是一种基于40年前发展的相溶解度技术,至今仍被普遍认为是最可靠且广泛使用的溶解度测量方法。当需要测定平衡溶解度时,可采用摇瓶法。
在选择溶解介质进行溶解度测量时,应根据研究目的考虑以下因素:表面活性剂的类型和浓度、缓冲液的离子强度,以及缓冲液中存在的反离子类型。当目的是预测吸收或生物利用度时,建议使用生物相关介质。当目的是支持溶出度试验的开发时,建议使用溶出介质。当评估化合物的pH值依赖性时,建议使用能够在较宽pH值范围内控制离子强度和反离子类型的缓冲液。当目的是用于BCS分类时,建议使用本版药典推荐的缓冲液。
样品制备:将过量固体原料药加入装有溶解介质的容器中,其中溶解介质的量无需精确测量。对于难溶性药物,建议在预估溶解度的基础上,每1ml溶解介质中额外加入1~2mg的原料药。可以通过在添加介质之前研磨样品或添加介质之后超声处理来增加原料药的表面积。[注意:这些方法可能会改变溶质的固体形态,使用时应谨慎。]建议每个条件的样品制备一式三份,以便至少获得3个溶解度结果。
平衡溶液:悬浮液应持续混合、搅拌或振荡促进固体溶解,一般而言,样品在24小时内可达到溶解平衡,但某些品种需要更长时间,因此须对平衡时间进行确认。溶解过程中需保持悬浮液的温度恒定(±0.5℃),取出溶液后应立即过滤、离心或沉淀来分离未溶解的固体样品。在取上清液时,应避免混入任何未溶解的固体,因为这会影响溶解度结果。如果必要,应立即进行稀释以避免溶质析出。在使用移液管之前,应使用样品溶液润洗以减少表面吸附的影响。过滤分离时,须选择适合的滤膜种类。对于极性或离子化物质,建议使用疏水型滤膜(如尼龙);对于非离子化物质,建议使用亲水性滤膜[如聚偏二氟乙烯(PVDF)或聚醚砜(PES)]。搅拌后不宜直接过滤,应在沉淀后进行,并弃去初滤液。在沉淀和离心过程中,仍需保持悬浮液的温度恒定(±0.5℃)。
应在不同时间点取样并测定溶液浓度,当连续测定的结果之间不再有显著变化(例如,24小时内的变化小于5%,或1小时内的变化小于0.2%),这表明溶液达到饱和(平衡)。为了确认所测得的表观溶解度确实为平衡溶解度,建议使用相同的程序对相同的悬浮液进行再次平衡(例如,再次混合24小时),然后重新测定以保证结果的一致性。
溶液分析:定量分析溶质浓度的方法应满足测量溶解度数据的预期目的,通常需验证分析方法的性能特征,包括专属性和范围等。在进行分析之前,可能需要稀释上清液或滤液,以确保其浓度在分析方法的线性范围内,避免溶质析出。可以使用紫外-可见分光光度法或高效液相色谱法来测定浓度,推荐使用高效液相色谱法,因为它有助于评估和监测稳定性。
在溶解度测量结束后,建议分析悬浮液中的过量固体,以确认固体形态是否保持不变。如果固体形态发生了变化,那么新固体形态的溶解度可能低于初始固体形态,观察到的溶解度是由于新的低溶解度形态所致,但这需要根据具体情况进行评估。评估固体形态的方法包括粉末X射线衍射法、拉曼光谱法、近红外光谱法或差示扫描量热法等。化学或物理上不稳定的溶质在平衡过程中不适合用摇瓶法测量平衡溶解度,例如,那些可能转化为低溶解度盐或多晶型形态的无定型药物,应采用一种表观溶解度测定方法进行分析。
溶解度结果报告:如果在溶解度测定中使用了非标准介质成分,应详细报告该成分。溶解度测定所用介质的离子强度应与溶解度结果一并计算和报告。取样分析时,应在溶解度测量的温度下记录上清液的pH值。当使用定义明确的标准介质时,建议不要调整介质的pH值以补偿溶质对pH值的影响;相反,应在平衡步骤结束时,在观察到的pH值和温度下报告溶解度。如果介质的pH值受到溶质的显著影响,并且需要获得特定pH值下的溶解度数据,建议在具有更高缓冲容量的介质中进行额外的溶解度测量。同时,应报告平衡过程中的平均温度和温度控制的精度。
报告的平衡溶解度的精密度应反映测量结果的一致性,并应包含基于至少3个独立样品的溶解度测量值的标准偏差。
2 表观溶解度测定方法
2.1 固有溶出测定法(转碟法)
固有溶出测定法是一种用于溶解度测量的方法。在进行溶解实验时,应持续进行直到溶解速度变得不显著(例如,24小时内小于5%,或者1小时内小于0.2%)。使用固有溶出装置进行测量时,应遵循摇瓶法在溶液分析和溶解度结果报告中的所有要求。
2.2 电位滴定法
酸碱电位滴定法是一种用于溶解度测量的方法,它基于由沉淀引起的滴定曲线中间的特征位移。滴定时,将准确体积的标准酸或碱溶液加入含有可电离物质和盐的溶液中,例如,0.15mol/L的氯化钾,以提高测量的准确性。为防止大气中的二氧化碳影响pH值,可以采用氩气喷射技术,这是一种将化学惰性气体(如氮气、氩气或氦气)通入液体的技术。在整个滴定过程中,使用玻璃电极连续监测pH值。通过绘制pH值与酸或碱消耗量的关系图,可以得到电位滴定曲线。
2.3 透射浊度法
透射浊度法是一种用于溶解度测量的方法。将化合物溶解在有机溶剂中,例如二甲基亚砜(DMSO),然后将溶液按一定间隔加入缓冲溶液中,以表征浊度的变化。首次通过光散射检测到浊度后,继续加入更多的溶液。并绘制体积与浊度的关系图。通过反向外推至沉淀开始点,可以估计溶解度。这种方法每天能够测量多达50~300个样品。然而使用DMSO等溶剂可能导致药物的溶解度在短时间内增加,从而测量的是动力学溶解度而非热力学溶解度,形成过饱和溶液,沉淀固体的晶体形态未知,除非将其从悬浮液中分离并进行表征。
2.4 物理评估法
对于溶解度极高的化合物,缺乏发色团的化合物或在溶液中难以定量的生物制剂和其他分子,物理评估法可用于评估表观溶解度。这种方法基于固体物质向溶液相转移的原理,通过监测重量损失和溶液物理性质(如折射率、密度、渗透压等)的变化来评估平衡状态。由于物理评估不涉及专属性和稳定性指示特性的检测,建议评价溶质的纯度和稳定性。此外,在采用这种方法进行溶解度测量时,应严格监测并控制溶剂的蒸发。
3.生物相关介质中的溶解度测量
使用简单的水相缓冲液来评估药物的水溶解度作为pH值的函数可能会低估生物利用度。因此,可以使用生物相关介质来模拟人类、犬类和反刍动物(如牛)体液中的溶解度,从而更准确地评估生物利用度。表1~表10是生物相关介质的示例。
表1 模拟人体空腹状态胃液(FaSSGF)的介质组成(37℃时pH值为1.6)
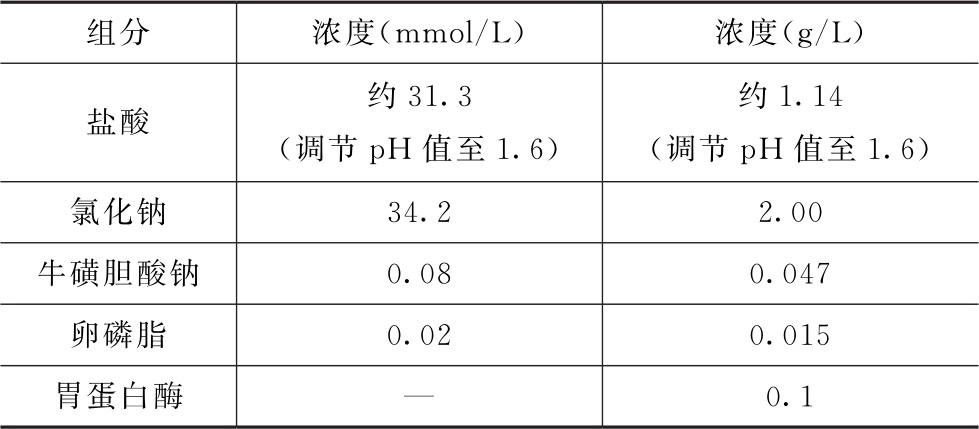
表2 模拟人体饱腹状态胃液(FeSSGF)的介质组成(37℃时pH值为5.0)
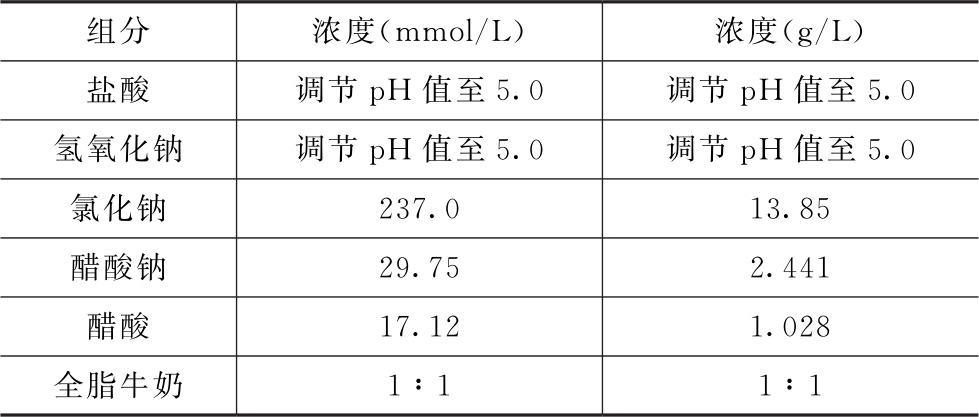
制备缓冲液,然后与牛奶以1∶1的比例混合。如有必要,调节pH值至5.0。
表3 模拟人体空腹状态肠液(FaSSIF-V2)的介质组成(37℃时pH值为6.5)
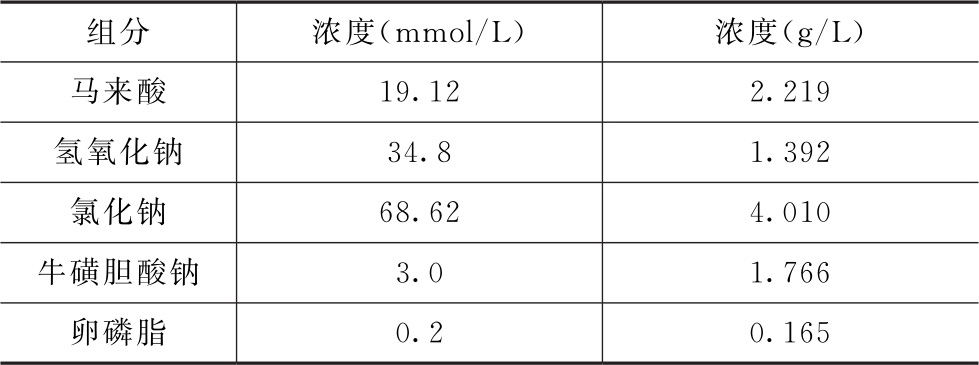
表4 模拟人体饱腹状态肠液(FeSSIF-V2)的介质组成(37℃时pH值为5.8)
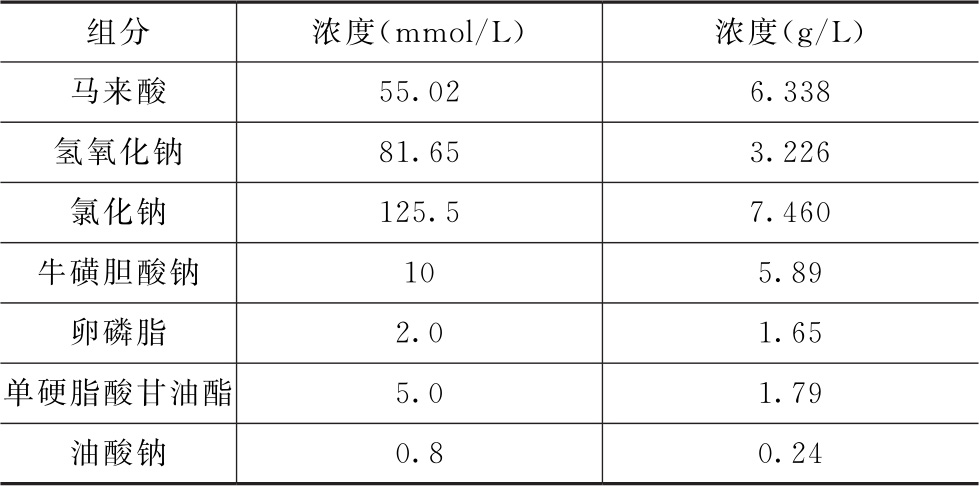
表5 模拟人体结肠液-近端结肠(SCoF2)的介质组成(37℃时pH值为5.8)
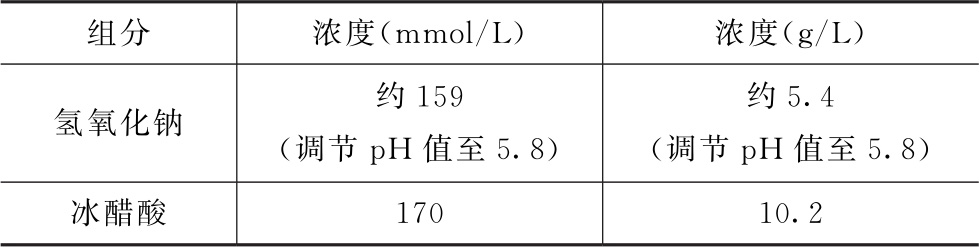
表6 模拟人体结肠液-远端结肠(SCoF1)的介质组成(37℃时pH值为7.0)
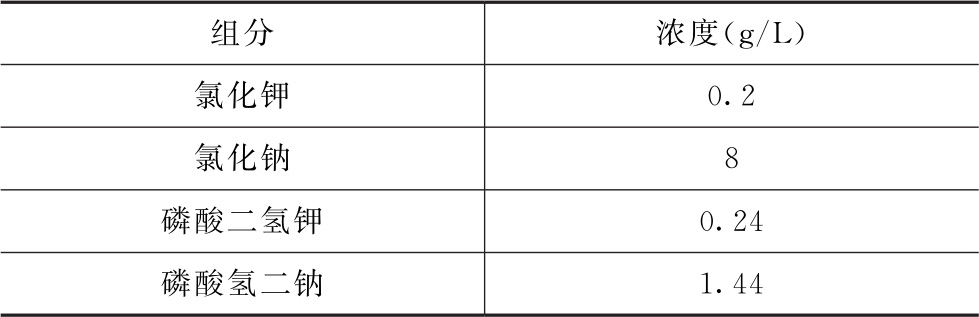
表7 模拟犬类空腹状态胃液(FaSSGFc pH 1.2~2.5)的介质组成(37℃时pH值为1.2~2.5)
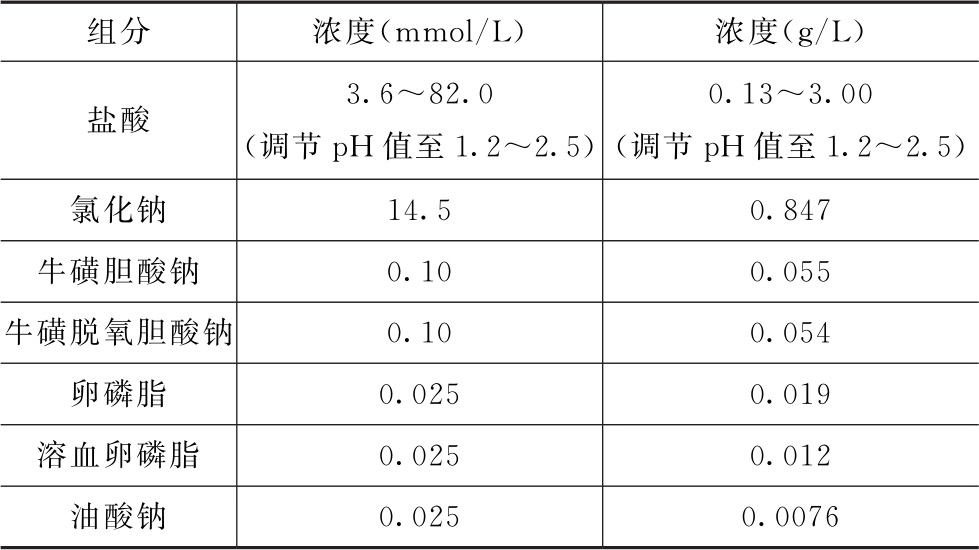
犬类胃的pH值可以有相当大的变化。由于不同研究中对犬类胃pH值的估计存在差异,因此应在1.2~6.5的范围内评估溶解度。可通过改变盐酸的用量来调节胃液的pH值,从而使pH值达到1.2~2.5的范围内。
表8 模拟犬类空腹状态胃液(FaSSGFc pH 2.5~6.5)的介质组成(37℃时pH值为2.5~6.5)
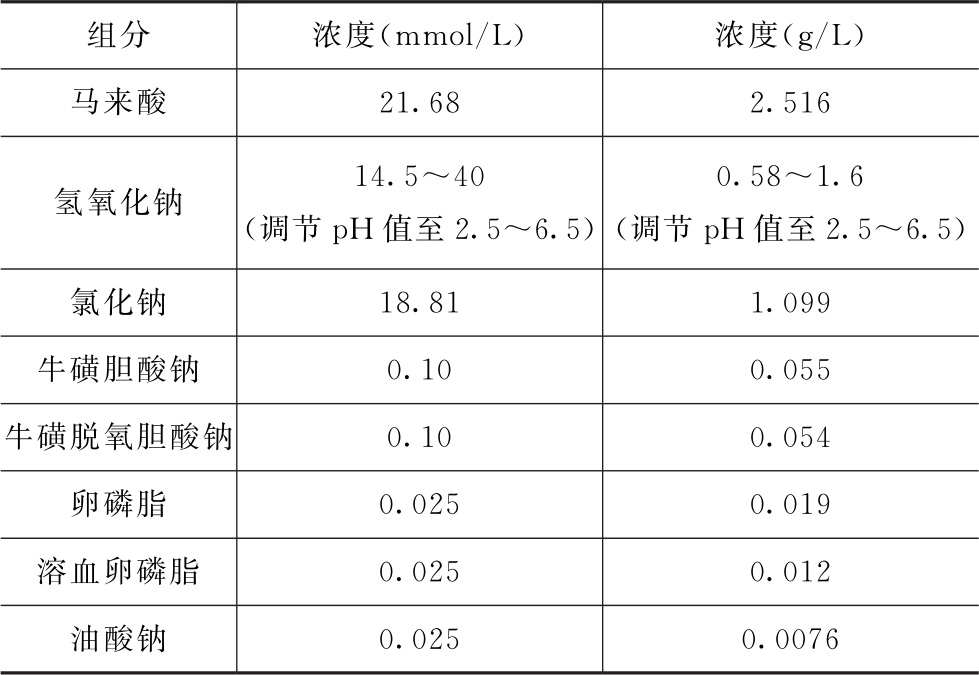
犬类胃的pH值可以有相当大的变化。由于不同研究中对犬类胃pH值的估计存在差异,因此应在1.2~6.5的范围内评估溶解度。可通过改变氢氧化钠的用量来调节胃液的pH值,从而使pH值达到2.5~6.5的范围。
表9 模拟犬类空腹状态肠液(FaSSIFc)的介质组成(37℃时pH值为7.5)
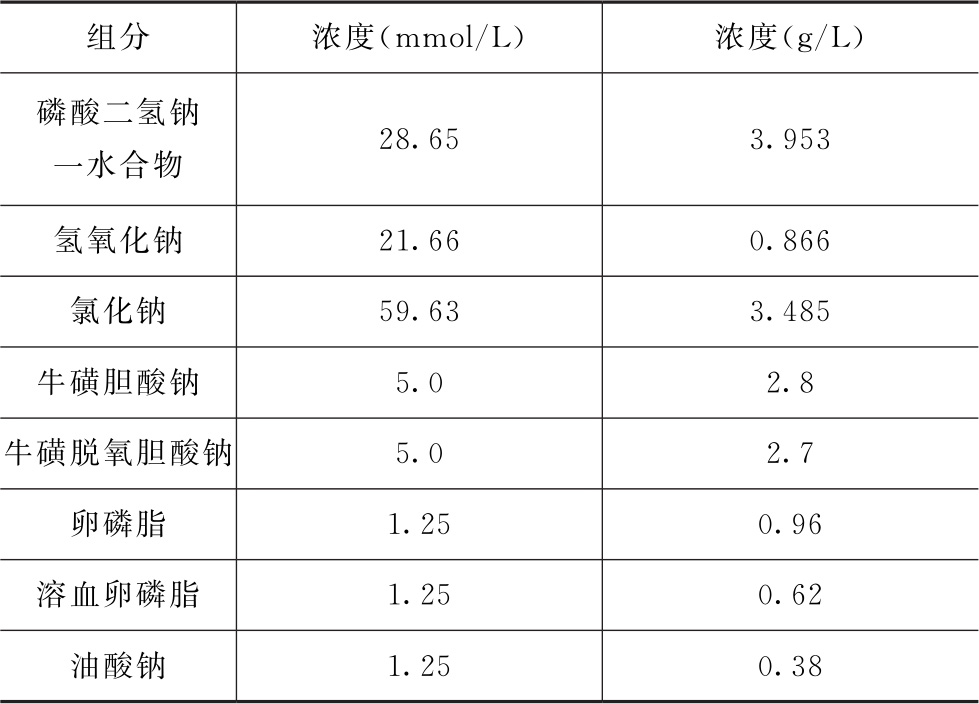
表10 模拟牛类胃液的介质组成(介质温度应设置为39℃)
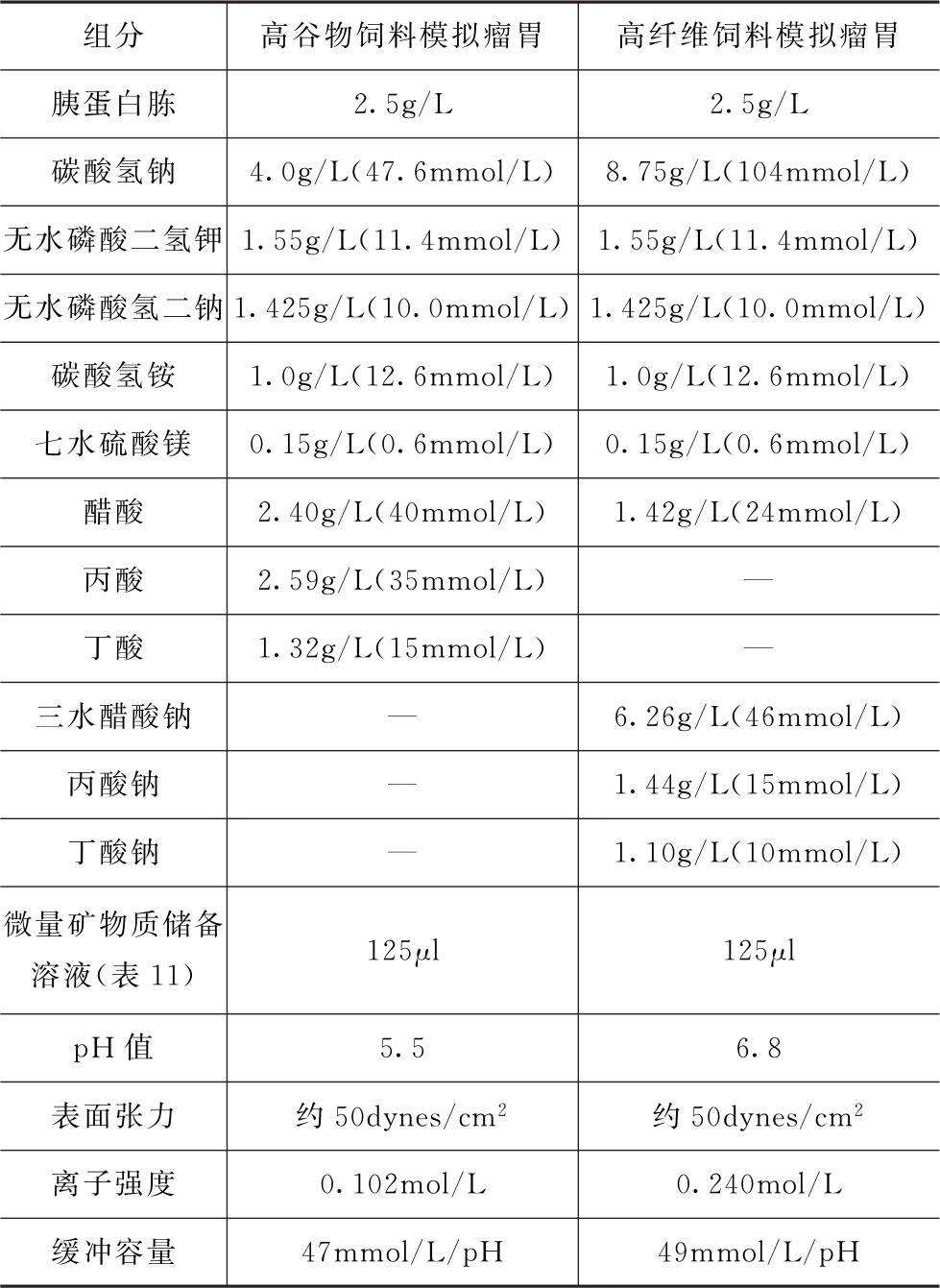
这里定义的介质适用于牛类以及其他反刍动物种类。健康的网胃-瘤胃的正常pH值范围是5.5~6.8。高谷物饲料通常会导致瘤胃的pH值较低(约为5.5),而高纤维饲料会导致瘤胃的pH值较高(约为6.8)。
在皱胃(真胃)中,pH值为2~3,与单胃动物和人类的情况相似。为了模拟皱胃,可以使用0.01mol/L盐酸(pH 2.0)、0.0033mol/L盐酸(pH 2.5)或0.001mol/L盐酸(pH 3.0)。反刍动物的肠道pH值与单胃动物和人类的相似。幽门处的pH值约为3.0,而回肠中增加到约7.5。为了模拟牛的肠液,可以使用上述为人类或犬类定义的模拟肠液之一。
表11 微量矿物质储备溶液的组成
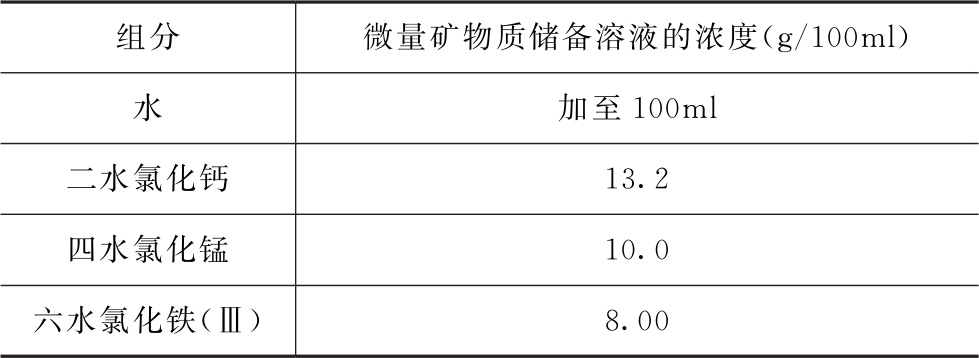
在进行生物相关溶解度测量时,溶解介质的温度应控制在±0.5℃,并遵循摇瓶法的要求,包括在多个时间点进行溶解度测量以确认达到平衡。药物的盐形式添加到溶解介质中,可能会显著改变介质的组成(如离子强度、pH值等)。因此,不应假定同一药物的盐形式和游离碱的溶解度相等,除非通过不同晶型固体独立测量来证实。
(c)蒲标网 - 中国药典、药品标准、法规在线查询 ( 津ICP备15007510号 )